DIE FIREBUSTERS
CHEMISCHES FEUERZEUG
Der ab 1810 an der Universität Jena tätige Johann Wolfgang Döbereiner gilt als Vordenker für die Entstehung des Periodensystems der Elemente und beschäftigte sich mit katalytischen Effekten. Vor allem seine Forschungen mit dem Edelmetall Platin machten ihn berühmt. Bekannt wurde er aber vor allem durch das nach ihm benannte erste „Chemische Feuerzeug“, welches auch Johann Wolfgang von Goethe beim Entzünden seiner Zigarren verwendet haben soll. Wie funktioniert das?
W
asserstoff (H) und Sauerstoff (O) können in Gegenwart von Platin (Pt) ohne äußere Zündquelle – unter Freisetzung von Energie – zu Wasser (H2O) verbrennen. Man nennt diesen Vorgang Platinkatalyse. Dabei geht folgende chemische Reaktion vor sich:
Wasserstoff (H) und Sauerstoff (O) können in Gegenwart von Platin (Pt) ohne äußere Zündquelle – unter Freisetzung von Energie – zu Wasser (H2O) verbrennen. Man nennt diesen Vorgang Platinkatalyse. Dabei geht folgende chemische Reaktion vor sich:
2 H2+ O22 H2O + Energie
Diese Reaktion läuft auch bei der Bildung von Knallgas – dort natürlich mit wesentlich größerer Intensität und Brisanz – ab (Knallgasreaktion) und wurde von Döbereiner zur Konstruktion eines sehr interessanten Feuerzeugs verwendet.
Funktionsweise
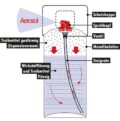
Sein Platinfeuerzeug funktioniert nun folgendermaßen: In einem mit verdünnter Schwefelsäure (H2SO4) gefüllten Glaszylinder befindet sich eine Glasglocke mit einem Kolben aus Zink (Zn). Bei der chemischen Reaktion wird Wasserstoffgas (H2) produziert:
Zn + H2SO 4 Zn SO4+ H2
Der Wasserstoff wird nun über ein Ventil über einen „Platinschwamm“ (feinverteiltes Platin) geleitet und entzündet sich aufgrund seiner katalytischen Reaktion mit Sauerstoff.
Literaturhinweis
WIDETSCHEK O.: DER GROSSE Gefahrgut-Helfer – Gefahren, richtiges Verhalten und Einsatzmaßnahmen bei Schadstoff-Unfällen; Leopold Stocker Verlag, Graz-Stuttgart, 2012. In diesem Lehrbuch werden die meisten der hier wiedergegebenen Experimente ausführlich beschrieben. Bestellungen über www.brandschutzforum.at – Shop.
WIDETSCHEK O.: Geschichte des Feuers – vom steinzeitlichen Feuerzeug bis zur Atombombe; Edition Brandschutzforum, 2020, Graz.
SEILNACHT T. und REHM M.: Experimente auf Video (pdf-Handbuch); www.seilnacht.com.

EXPERIMENT: EXPLODIERENDE SEIFENBLASEN
Platin als Katalysator
Beim Verbrennungsvorgang spielen sogenannte Katalysatoren eine große Rolle. Es sind dies reaktive Atome, Moleküle und Molekülbruchstücke, welche die Rolle eines „Heiratsvermittlers“ für die Verbindung von Atomen und Molekülen übernehmen. Bekannte Katalysatoren sind Edelmetalle, welche die Aktivierungsenergie bei der Verbrennung herabsetzen.
Materialien:
- Wasserstoff (Gasflasche)
- Stativ mit Klemme
- Glasdüse mit Rückschlagsicherung
- Platin-Palladium (Pt-Pd)-Katalysator im Kugelform (Fa. Hedinger, Stuttgart) oder gewendelter Platindraht (Fa. PlatinAustria)
- Tiegelzange bzw. Pinzette
Anmerkung:
In der Glasdüse sollte vor Durchführung des Versuches eine Rückschlagsicherung aus Eisenwolle eingebaut werden!
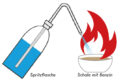
Versuch:
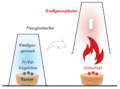
Mit Hilfe einer Tiegelzange wird ein Pt-Pd-Katalysatorkügelchen oder ein gewendelter Platindraht in das ausströmende Wasserstoffgas (in etwa 5 cm über der Düsenöffnung) gehalten. Nach einer Weile beginnt das Edelmetall, wie von Zauberhand, zu glühen und entzündet den Wasserstoff mit einem Knall.
Anmerkung:
Wasserstoff entzündet sich normalerweise bei etwa 585 °C, kann jedoch durch die Platinkatalyse schon bei Zimmertemperatur (20 °C) brennen.
Erklärung:
Platin ist in der Lage, Wasserstoff zu absorbieren, wobei der molekulare Wasserstoff (H2) teilweise in reaktionsfreudigen atomaren Wasserstoff (H*) umgewandelt wird. Dadurch kann die chemische Reaktion eingeleitet und der Wasserstoff gezündet werden. Das Platin ist als Katalysator dabei aktiv beteiligt und geht Zwischenverbindungen ein, liegt aber am Ende der chemischen Reaktion jedoch wieder unverändert vor.
Sicherheitshinweise:
Das Tragen einer Schutzbrille ist bei diesem Versuch obligatorisch. Vor dem eigentlichen Experiment soll die mögliche Höhe der Wasserstofflamme getestet werden. Der Versuch ist nur von erfahrenem Fachpersonal und vorwiegend unter einem Abzug bzw. nur in voluminöseren Räumen durchzuführen. Außerdem sollte eine vorhandene Raumlüftung zur Abführung des entweichenden Wasserstoffs eingeschaltet werden.
Hinweise zur Lagerung von Platin: Drähte, Bleche Schwämme mit Platin beschichtete Trägermaterialien sollen gut verschlossen aufbewahrt werden, weil sie in der Lage sind, Alkoholdämpfe und Wasserstoffgas zu entzünden.

Text: Dr. Otto Widetschek Fotos: Ewald Hofer; Grafik: Owid

Autor:
ELFR Dr. Otto Widetschek

Die Redaktion ersucht, den Warnhinweis zu beachten. Alle dargestellten Versuche bergen bei unsachgemäßer Ausführung Gefahren in sich. Bei Unfällen wird seitens der Redaktion keine Haftung übernommen.